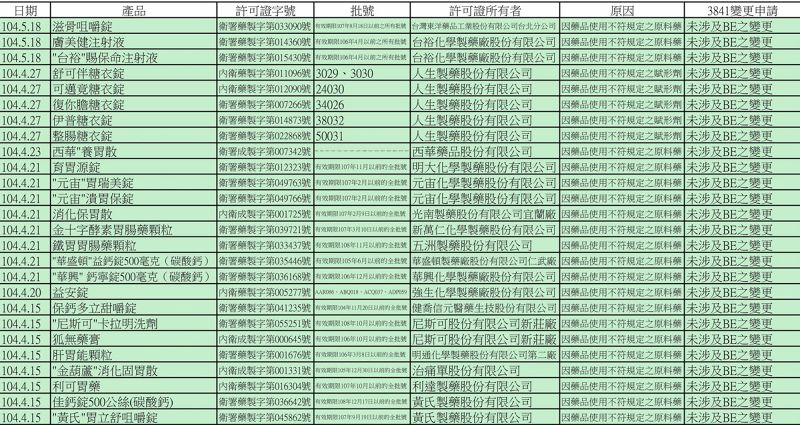
林淑芬強調,從這份2013年1月7日衛生署的公文可以發現,衛生署明確知悉藥商有違法未經核准就自行變更藥品成分情事,且「經常發現」,但衛生署卻「明知而不作為」,怠忽職守未依法查核處分廠商,甚至還「作弊」提醒違法廠商趕快補正。
2008年前核准之問題藥品 可以臨床經驗取代BE報告
之後衛生署於2013年3月清查出3841件未經許可自行變更製藥成分的藥品品項,當時的食品藥物管理局長、現任行政院食安辦公室主任康照洲於同年3月5日邀集專家學者及製藥公會、協會幹部召開「台灣藥品優質化策略討論會」,會議由康照洲主持,共同商討如何處理、解決3841件違法自行變更成分的藥品問題。會中製藥公、協會與會幹部建議,以2008年為分水嶺,該年之後核准的藥品自行變更成分本應做BE臨床試驗者,需補執行並補BE報告;至於該年之前的舊產品應就療效和安全上兩面向來考量,「如果長期存在無嚴重安全問題,又無療效爭議,應該可以接受」。
最後該次名為「台灣藥品優質化策略討論會」,實為將問題藥品就地合法化會議,做出決議,「藥品上市5年為合理之臨床使用經驗;2009年1月1日以前製造販售之藥品,如無重大嚴重不良反應或療效不等事件發生者,『得以其臨床經驗取代BE報告』;又2009年1月1日以後製造販售之藥品,2年內需完成BE試驗報告,所完成之BE報告留廠備查」,屆時食藥署若抽審未通過者,應切結不製造、販售,未切結者,廢止該項藥品許可證。
衛生署食品藥物管理局隨即在2013年3月28日,將會議決議行文三大製藥公、協會,公文中白紙黑字違法同意藥商就地合法。該局並於同年的9月17日將改制後兼代食藥署的衛福部常次許銘能報告「台灣藥品優質化執行後續策略」的執行現況,許銘能亦同意了此一放水讓藥商就地合法化作法。至2013年底原本清查的3841件問題藥品案,其中有2929件、逾7成5以「未涉及BE變更」直接予以合法,最後只有5件需重作BE臨床試驗報告。


但林淑芬指出,如今爆發藥品安全風暴,在衛福部食藥品網站上公布,今年被要求下架「產品回收」的100餘件問題藥品中,就有超過4分之1是列名當年3841件問題藥品的黑名單中,且最後就已「未涉及BE變更」輕騎過關,衛福部、食藥署明顯包庇、圖利違法藥商,罔顧民眾藥品安全。